Ścieżka audytu: Zapewnienie identyfikowalności i zgodności
W wielu branżach, szczególnie w większych organizacjach, utrzymywanie niezmienialnego śladu audytowego wszystkich modyfikacji bazy danych jest nie tylko dobrą praktyką, ale wymogiem prawnym. Przepisy takie jak US FDA Title 21 CFR Part 11 nakładają na firmy z sektora medycznego i farmaceutycznego obowiązek ścisłego prowadzenia dokumentacji i śladów audytowych. Jednak nawet bez takich zobowiązań prawnych wiele firm decyduje się na wdrożenie śladów audytowych w celu zwiększenia identyfikowalności, odpowiedzialności i integralności danych.
Niezmienny dziennik audytu PartsBox
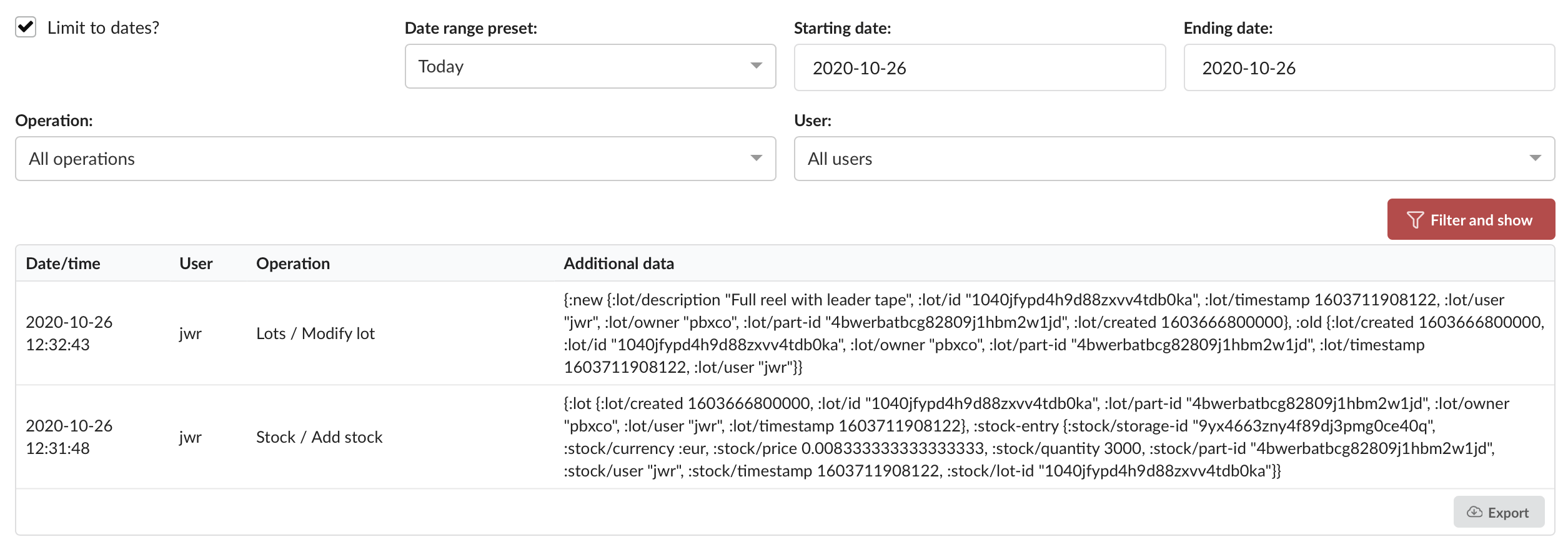
PartsBox oferuje solidną, niezmienną funkcję ścieżki audytu, która automatycznie rejestruje szczegółową historię każdej zmiany dokonanej w bazie danych. Każdy wpis ścieżki audytu zawiera:
- Znacznik czasu: Dokładna data i godzina wystąpienia modyfikacji.
- Użytkownik: Konto użytkownika, które wykonało operację, co pozwala na indywidualną odpowiedzialność.
- Operacja: Konkretna wykonana akcja, taka jak utworzenie, aktualizacja lub usunięcie rekordu.
- Typ rekordu: Typ rekordu, którego dotyczy zmiana, np. część, lokalizacja przechowywania, projekt lub zamówienie.
- ID rekordu: Unikalny identyfikator rekordu, którego dotyczy zmiana.
- Zmiany: Szczegółowe informacje o tym, co dokładnie zostało zmienione, w tym stare i nowe wartości.
Ten kompleksowy dziennik audytu (audit trail) zapewnia, że żadna modyfikacja nie pozostanie niezauważona i że zawsze istnieje jasna, krok po kroku historia ewolucji bazy danych w czasie.
Eksport i podpis dla zgodności z przepisami
Aby ułatwić zgodność z przepisami i usprawnić audyty, PartsBox umożliwia łatwy eksport danych ścieżki audytu w ustandaryzowanym formacie. Te wyeksportowane dane mogą być następnie podpisane cyfrowo przy użyciu bezpiecznych metod kryptograficznych, zapewniając dodatkową warstwę integralności i autentyczności.
Połączenie niezmienialnego dziennika zdarzeń (audit trail) i podpisanych eksportów sprawia, że PartsBox doskonale nadaje się do użytku w branżach regulowanych. Zapewnia niezbędne narzędzia do spełnienia rygorystycznych wymagań dotyczących prowadzenia dokumentacji i wykazania zgodności audytorom oraz organom regulacyjnym.
Dostępność i ceny
Funkcja dziennika audytu (audit trail) jest zawarta w planie Medical/Pharma PartsBox, który jest dostosowany do potrzeb firm z branży medycznej i farmaceutycznej. Dla organizacji z innych sektorów, które wymagają funkcjonalności dziennika audytu, jest ona dostępna na życzenie. Prosimy o kontakt z naszym zespołem sprzedaży w celu omówienia konkretnych wymagań i wyceny.
Dzięki ścieżce audytu PartsBox możesz mieć pewność co do integralności i identyfikowalności danych o stanach magazynowych części. Niezależnie od tego, czy chodzi o zgodność z przepisami, czy po prostu o lepsze zarządzanie danymi, ta funkcja stanowi niezbędne narzędzie do zarządzania częściami elektronicznymi w dzisiejszym złożonym i wymagającym środowisku biznesowym.